A regeneração tecidual é a capacidade de um organismo reparar ou substituir células, tecidos e até órgãos danificados, restaurando sua função original. Esse processo pode ocorrer naturalmente, como parte da resposta biológica à lesão, ou ser induzido por técnicas médicas e biotecnológicas.
Embora alguns animais, como salamandras e estrelas-do-mar, apresentem regeneração impressionante, os seres humanos possuem capacidade mais limitada. No entanto, avanços recentes na biomedicina vêm ampliando as possibilidades de estimular e direcionar a regeneração, com impacto direto na medicina regenerativa.
Como funciona biologicamente a regeneração tecidual?
A regeneração tecidual envolve eventos celulares e moleculares coordenados. Inicialmente, células especializadas percebem o dano e ativam sinais químicos, chamados fatores de crescimento, que promovem a proliferação celular. Essas células podem ser progenitoras do próprio tecido ou células-tronco indiferenciadas, particularmente na medula óssea.
Ao longo do processo, ocorre remodelação da matriz extracelular, revascularização e integração das novas células ao tecido original. Diferente da cicatrização, que muitas vezes resulta em fibrose e perda funcional, a regeneração busca restaurar a arquitetura e a função originais.
Qual a diferença entre regeneração e cicatrização?
A cicatrização é um mecanismo rápido e eficiente para fechar feridas, mas geralmente compromete a função do tecido, formando cicatrizes cheias de colágeno rígido. Já a regeneração substitui o tecido danificado por uma estrutura idêntica à original.
Por exemplo, o fígado humano é capaz de regenerar parte de sua massa após lesões, preservando sua função. Em contrapartida, o músculo cardíaco, após um infarto, tende a formar tecido fibroso que reduz a capacidade contrátil. Compreender essa diferença é essencial para desenvolver estratégias que evitem fibrose e favoreçam a regeneração.
Para mais detalhes sobre as diferanças, ler nosso artigo específico nesse link.
Quais tecidos humanos se regeneram naturalmente?
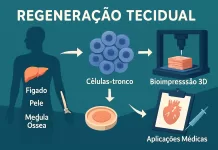
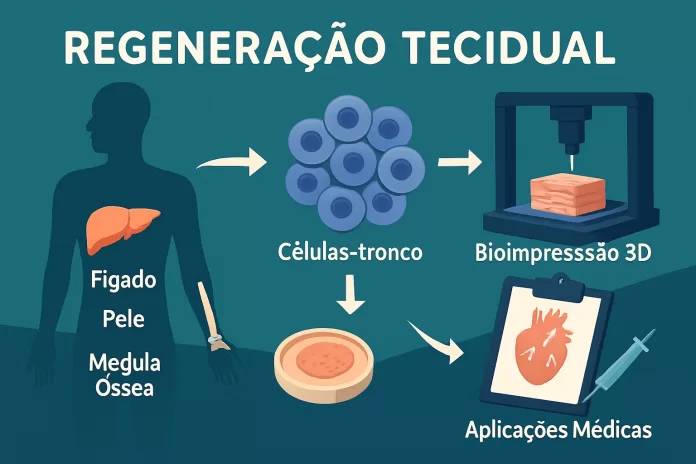
Embora não tenhamos o mesmo potencial regenerativo de alguns animais, o corpo humano mantém certas capacidades. Entre os exemplos mais notáveis estão a regeneração do fígado, da pele e da medula óssea.
O fígado pode recuperar até 70% de seu volume perdido. A pele apresenta renovação constante, permitindo reparos diários contra microlesões. Já a medula óssea mantém a produção contínua de células sanguíneas ao longo da vida. Essas capacidades naturais inspiram terapias que visam ampliar o potencial regenerativo de tecidos menos responsivos.
Qual o papel das células-tronco na regeneração?
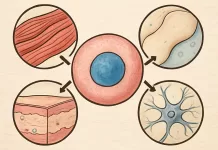
As células-tronco são protagonistas na regeneração tecidual. Elas podem se dividir indefinidamente e se diferenciar em diversos tipos celulares. Existem três principais fontes: embrionárias, adultas e induzidas por reprogramação genética (iPSCs).
As células-tronco adultas, como as mesenquimais, são encontradas em tecidos como medula óssea e gordura, e têm sido usadas em estudos para tratar lesões musculares, articulares e cardíacas. Manipular essas células permite criar terapias personalizadas para restaurar funções perdidas.
O que é engenharia de tecidos?
A engenharia de tecidos combina princípios da biologia celular com tecnologias de biomateriais para criar estruturas funcionais que substituem ou regeneram tecidos. Normalmente, utiliza-se um arcabouço tridimensional (scaffold) biocompatível, povoado com células e nutrido em condições controladas.
Esse campo já produziu pele artificial para queimaduras graves, cartilagem para articulações e até protótipos de órgãos bioimpressos em 3D. O desafio atual é criar tecidos vascularizados e integráveis ao corpo humano, evitando rejeição imunológica.
Como terapias gênicas e fatores de crescimento ajudam?
A terapia gênica busca inserir, modificar ou silenciar genes para estimular a regeneração. Pode ativar genes que promovem proliferação celular ou suprimir genes que favorecem fibrose.
Paralelamente, o uso de fatores de crescimento, como o PDGF e o VEGF, vem sendo estudado para acelerar a reparação e promover formação de novos vasos sanguíneos. Esses métodos têm sido explorados em tratamentos para úlceras crônicas e lesões musculares.
Quais são as aplicações médicas atuais?
A regeneração tecidual já encontra aplicações em várias especialidades médicas. Na ortopedia, auxilia na reconstrução de cartilagem em lesões articulares. Na dermatologia, viabiliza enxertos de pele cultivados em laboratório. Na cardiologia, investiga-se o uso de células-tronco para reparar tecido cardíaco pós-infarto.
Na oftalmologia, terapias regenerativas restauram córneas danificadas. Além disso, técnicas combinando biomateriais e fatores de crescimento estão sendo testadas para regenerar nervos periféricos.
Quais são as principais limitações e desafios?
Apesar dos avanços, a regeneração tecidual enfrenta obstáculos importantes. A integração de novos tecidos ao organismo nem sempre é bem-sucedida, e a resposta imunológica pode provocar rejeição. Além disso, o risco de crescimento celular descontrolado, levando a tumores, exige rigor na segurança das terapias.
Outro desafio é a produção em larga escala, já que muitas técnicas ainda dependem de processos caros e complexos. É fundamental desenvolver biomateriais acessíveis e protocolos clínicos padronizados para ampliar o acesso.
O que esperar do futuro da regeneração tecidual?
O futuro combina biotecnologia, inteligência artificial e medicina personalizada. A bioimpressão 3D de órgãos, a integração de nanomateriais que liberam fatores de crescimento de forma controlada e o uso de edição genética de alta precisão (como CRISPR-Cas9) estão entre as tendências mais promissoras.
Com a compreensão crescente dos mecanismos biológicos envolvidos, espera-se que terapias regenerativas se tornem rotina hospitalar, oferecendo soluções mais eficazes e menos invasivas. Mas ainda vai levar algumas décadas para atingir esse grau de maturidade.
Conclusão
A regeneração tecidual representa um campo científico em constante evolução, com potencial para transformar a medicina contemporânea. Ao compreender seus fundamentos e desafios, é possível visualizar um futuro no qual danos antes irreversíveis possam ser reparados de forma funcional.
A união entre pesquisa básica, inovação tecnológica e ética será decisiva para que seus benefícios alcancem mais pacientes, melhorando qualidade e expectativa de vida.
Referências
- Zakrzewski, W., Dobrzyński, M., Szymonowicz, M., & Rybak, Z. (2019). Stem cells: past, present, and future. Stem Cell Research & Therapy, 10(68). https://doi.org/10.1186/s13287-019-1165-5
- Mao, A. S., & Mooney, D. J. (2015). Regenerative medicine: Current therapies and future directions. Proceedings of the National Academy of Sciences, 112(47), 14452–14459. https://doi.org/10.1073/pnas.1508520112
- Murphy, S. V., & Atala, A. (2014). 3D bioprinting of tissues and organs. Nature Biotechnology, 32, 773–785. https://doi.org/10.1038/nbt.2958
- Yamada, K. M., & Cukierman, E. (2007). Modeling tissue morphogenesis and cancer in 3D. Cell, 130(4), 601–610. https://doi.org/10.1016/j.cell.2007.08.006





















[…] Para mais detalhes, ler nosso artigo específico sobre regeneração nesse link. […]